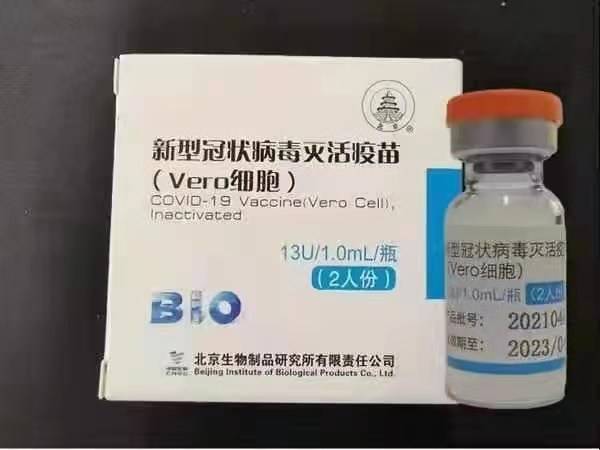
Sinopharm (Пекін): BBIBP-CorV
ЕТАП 1
1 Випробування
ChiCTR2000032459
Китай
ЕТАП 2
2 випробування
NCT04962906
Аргентина
ChiCTR2000032459
Китай
ЕТАП 3
6 випробувань
NCT04984408
ChiCTR2000034780
Об'єднані Арабські Емірати
NCT04612972
Перу
NCT04510207
Бахрейн, Єгипет, Йорданія, Об'єднані Арабські Емірати
NCT04560881, BIBP2020003AR
Аргентина
NCT04917523
Об'єднані Арабські Емірати
Схвалення
Список ВООЗ щодо екстреного використання 59 країн
Ангола, Аргентина, Бахрейн, Бангладеш, Білорусь, Беліз, Болівія (багатонаціональна держава), Бразилія, Бруней -Даруссалам, Камбоджа, Камерун, Чад, Китай, Коморські острови, Єгипет, Екваторіальна Гвінея, Габон, Гамбія, Грузія, Грузія, Грузія 、 Іран (Ісламська Республіка) 、 Ірак 、 Йорданія 、 Киргизстан 、 Лаоська Народно -Демократична Республіка
Ліван, Малайзія, Мальдіви, Мавританія, Авріцій, Монголія, Чорногорія, Марокко, Мозамбік, Намібія, Непал, Нігер, Північна Македонія, Пакистан, Парагвай, Перу, Філіппіни, Республіка Конго, Енегал, Сербія, Сейєр Острови 、 Сомалі 、 Шрі -Ланка 、 Таїланд 、 Тринідад і Тобаго 、 Туніс 、 Об'єднані Арабські Емірати 、 Венесуела (Боліваріанська Республіка) 、 В'єтнам im Зімбабве
Sinopharm BBIBP-CorV COVID-19-це інактивована вакцина, вироблена з вирощених культурою частинок вірусу, які не мають патогенної здатності. Цей кандидат на вакцину був розроблений Sinopharm Holdings та Пекінським інститутом біопрепаратів.
Вакцина Sinopharm BBIBP-CorV працює, дозволяючи імунній системі виробляти антитіла проти коронавірусу SARS-CoV-2. Інактивовані вірусні вакцини використовуються протягом десятиліть, такі як вакцина проти сказу та вакцина проти гепатиту А. Ця технологія розвитку успішно застосовується до багатьох відомих вакцин, таких як вакцина проти сказу.
Штам SARS-CoV-2 Sinopharm (штам WIV04 та бібліотечний номер MN996528) був виділений від пацієнта в лікарні Цзіньйаньтань у місті Ухань, Китай. Вірус розмножували в культурі компетентною клітинною лінією Vero, і супернатант інфікованих клітин інактивували β-пропіолактоном (1: 4000 об./Об., Від 2 до 8 ° С) протягом 48 годин. Після очищення клітинного сміття та ультрафільтрації була проведена друга інактивація β-пропіолактону за тих самих умов, що і перша інактивація. За даними ВООЗ, вакцину адсорбували на 0,5 мг галуну та завантажували у попередньо заповнені шприци у 0,5 мл стерильного фосфатно-сольового розчину без консервантів.
31 грудня 2020 року Державна адміністрація з лікарських засобів оголосила про схвалення експериментальної вакцини, розробленої компанією Sinopharm.
7 травня 2021 року Всесвітня організація охорони здоров’я оголосила про схвалення вакцини. Список екстренного використання ВООЗ дозволив країнам прискорити власні регуляторні дозволи на імпорт та введення вакцини проти COVID-19. Консультативна група експертів ВООЗ зі стратегій імунізації також завершила огляд вакцини. На підставі всіх наявних даних ВООЗ рекомендує дві дози вакцини з інтервалом у три -чотири тижні для дорослих від 18 років. Ефективність вакцини проти симптоматичної та госпіталізованої хвороби оцінюється у 79% для всіх вікових груп разом узятих.
Американська медична асоціація опублікувала "Рандомізоване клінічне випробування: вплив 2-х інактивованих вакцин проти SARS-CoV-2 на симптоматичну інфекцію COVID-19 у дорослих" 26 травня 2021 року, зробивши висновок, що "у цьому попередньо визначеному проміжному аналізі рандомізованого клінічного випробування, дорослі 2 інактивовані вакцини проти SARS-CoV-2, які були введені в цьому попередньо визначеному проміжному аналізі рандомізованих клінічних випробувань, значно знизили ризик симптоматичного COVID-19, а серйозні побічні ефекти були рідкістю ". У цьому рандомізованому дослідженні 3 фази у дорослих ефективність 2 інактивованих цільних вакцин проти вірусу у симптоматичних випадках COVID-19 становила 72,8% та 78,1% відповідно. 2 вакцини мали рідкісні серйозні побічні явища з подібною частотою, ніж контрольна група тільки для галунів, і більшість з них не мали відношення до вакцинації. Дослідницький аналіз виявив, що 2 вакцини викликали вимірювані нейтралізуючі антитіла, подібні до результатів випробування фази 1/2.
Робоча група ВООЗ SAGE опублікувала огляд вакцини Sinopharm/BBIBP від COVID-19 10 травня 2021 р. Вакцина від COVID-19 від GAVI містить монітор у флаконі з вакциною, який повідомляє медичним працівникам про те, чи правильно зберігалася вакцина і чи вона не піддавалася впливу. перегрівання. В результаті, про пошкодження, повідомляє GAVI 14 травня 2021 р. Розумні етикетки виробництва компанії Zebra Technologies та виробництва Temptime Corporation складаються з кола з більш світлим кольоровим квадратом посередині, виготовленим з безбарвного хімікату, який з часом незворотно змінює колір . Він стає темнішим, щоб візуально вказувати на сукупний вплив тепла. Після того, як флакон піддався нагріванню за межами оптимального діапазону зберігання, квадрат стає темнішим за коло, що вказує на те, що вакцину більше не слід використовувати.
Реєстраційний номер національної бібліотеки ліків від вакцин проти ліків проти вакцини проти коронавірусу COVID-19: DB15807.